- +23%* d’absorption du fer cliniquement prouvée
- Sans troubles digestifs
- Sans goût de fer
Complément alimentaire de Fer bisglycinate
Efficacité de notre complément alimentaire de Fer
- +23%d’absorption du fer grâce à notre souche lactique brevetée
- 100%des apports recommandés en fer dans une seule gélule


Les routines associées à notre Fer
Découvrez nos produits aux bienfaits complémentaires.
Pourquoi prendre le complément alimentaire Fer Nutri&Co ?
Loin des formules classiques souvent responsables de troubles digestifs, notre formule associe du fer bisglycinate à une souche probiotique capable d'optimiser son absorption. Elle est complétée par de la vitamine C et de vitamine B9 sous forme de folates.
Du fer sans les effets secondaires indésirables
Notre formule s’articule autour du couple bisglycinate de fer (Breveté TRAACS®) et souche lactique (Lactobacillus plantarum 299v®) qui constitue une rupture dans l’approche de la supplémentation ferrique.
Plutôt que de résoudre l’équation du déficit par un excès d’apport en fer, notre formule est conçue pour améliorer l’absorption du précieux minéral. Cette approche inédite permet d’éviter les méga-doses en fer et les désagréments qui y sont liés, notamment les troubles digestifs.
Les effets de notre complément alimentaire Fer
Le Fer
- Joue un rôle dans le processus de division cellulaire.
- Contribue à des fonctions cognitives normales, à la réduction de la fatigue et à la formation normale de globules rouges et d'hémoglobine.
La vitamine C
- Augmente l'absorption de fer.
La vitamine B9 (folates)
- Contribue à la croissance des tissus maternels durant la grossesse.
Fer, folates et vitamine C
- Contribuent à réduire la fatigue.
Valeur nutritionnelle du Fer bisglycinate (mg) 1 gélule % des AR* Lactobacillus plantarum 299vxc 66mg
10mds UFC**
- Vitamine C 12mg 15 Ferrochel® : Fer Chélaté
Bisglycinate labellisé TRAACS®
dont Fer élément
70mg
14mg
100
Folates (Vitamine B9) 216μg 108 *Apports de Référence
**Unité Formant Colonie
23% d'absorption en plus cliniquement prouvée
Cela n’a l’air de rien, mais les études cliniques sur produits finis sont rares en Nutra. En ce qui concerne notre Fer breveté, ce ne sont pas moins de 3 études qui démontrent :
- la bonne tolérance de notre Fer notamment en matière digestive,
- son efficacité avec une absorption accrue d’au moins 23% notamment chez les femmes,
- et l’amélioration des marqueurs biologiques associés au fer (ferritine et hémoglobine).
Bien plus qu’une simple formule de Fer...
Parce que les risques de déficit en fer touchent des populations spécifiques, notamment les femmes enceintes et les sportifs d’endurance, notre formule répond aussi à leurs besoins. Elle apporte une dose quotidienne de 216 μg de folates, forme biodisponible d’acide folique, essentiels pour ces populations.
De la vitamine C en synergie avec le Fer
Une seule gélule de fer par jour !
Notre formule prend place dans une seule petite gélule par jour. Elle est étudiée pour éviter le goût métallique et ainsi faciliter au maximum la prise.
Bienfaits de notre Fer Bisglycinate
Le Fer
- Joue un rôle dans le processus de division cellulaire.
- Contribue à des fonctions cognitives normales, à la réduction de la fatigue et à la formation normale de globules rouges et d'hémoglobine.
La vitamine C
- Augmente l'absorption de fer.
La vitamine B9 (folates)
- Contribue à la croissance des tissus maternels durant la grossesse.
Fer, folates et vitamine C
- Contribuent à réduire la fatigue.
Le fer est l’oligo-élément le plus abondant de notre organisme. Il est essentiel à l’oxygénation de notre sang et intervient dans de nombreuses fonctions comme les fonctions cognitives, le système immunitaire, le métabolisme et est essentiel au bon développement de l’enfant in utero.
Si un déficit en fer ne signifie pas pour autant carence en fer ni anémie, il est préférable d’y répondre avant que cela ne devienne problématique. Ainsi, les compléments alimentaires s’avèrent être une solution efficace. Notre formule de fer s’articule autour d’une souche lactique et d’un dosage raisonnable en fer bien toléré (elle limite ainsi les désagréments bien souvent associés) tout en optimisant l’absorption (vitamine C).
Des bienfaits anti-fatigue
Bien souvent, une analyse par simple prise de sang est la première étape pour identifier l’origine d’une fatigue chronique. En fonction du taux de ferritine sanguin, les bienfaits du fer en supplémentation peut se révéler une réponse efficace et adaptée.
Des bienfaits majeurs pour les femmes et sportifs d’endurance
Si le déficit en fer est relativement courant dans la population générale, il touche très majoritairement les femmes pendant la grossesse et les sportifs d’endurance extrême. Notre formule a été conçue pour subvenir aux besoins en fer de ses populations en leur apportant en plus des folates, un nutriment essentiel qui leur est recommandé.
Ingrédients et analyses
- Fer Bisglycinate labellisé TRAACS®
Liste des ingrédients
Valeur nutritionnelle du Fer bisglycinate (mg) 1 gélule % des AR* Lactobacillus plantarum 299vxc 66mg
10mds UFC**
- Vitamine C 12mg 15 Ferrochel® : Fer Chélaté
Bisglycinate labellisé TRAACS®
dont Fer élément
70mg
14mg
100
Folates (Vitamine B9) 216μg 108 *Apports de Référence
**Unité Formant Colonie
Ingrédients : Amidon de maïs, Gélule gastro-résistante (gélifiants : hydroxypropylméthylcellulose, pectine), Bisglycinate de fer (Ferrochel®) labellisé TRAACS® (The Real Amino Acid Chelate System), Probiotique : Lactobacillus plantarum 299v® (DSM 9843), Vitamine C (acide L-ascorbique), Quatrefolic® [(6S)-5-Méthyltétrahydrofolate, sel de glucosamine].
Analyses
Notre promesse de transparence passe aussi par la publication des analyses qualité :
Encapsulation (mise en gélules) - Exden
Fabrication : Nantes, FranceEXDEN est un laboratoire français spécialiste des compléments alimentaires à base de probiotiques.Souche Lp299v® - Probi
Fabrication : Redmond, USA - Lieu de culture : Redmond, Washington, USA - Centre de Recherche : Malmö, Suède Probi est le producteur de la souche Lactobacillus Plantarum 299v (LP299v). LP299v bénéficie de plus de 200 publications scientifiques, dont 65 études cliniques dont 3 réalisées spécifiquement sur notre formule.Bisglycinate de Fer (Breveté TRAACS®) - Albion Laboratories, Inc.
Ogden, États-UnisAlbion Minéral est le pionnier mondial en production de minéraux chélatés. Leurs chélates sont produits via des procédés de fermentation non polluants de dernière génération.Quatrefolic® (folates) - Gnosis
Fabrication : Milan, ItalieGnosis met en œuvre des processus de biotransformation (fermentation) pour concevoir des actifs nutritionnels dans le but d’améliorer la santé et le bien-être de l’Homme.Vitamine C - Natural
Verrières-en-Anjou, FranceNatural est une entreprise française spécialisée dans la distribution d'ingrédients naturels pour l'industrie nutraceutique.

Conseils d’utilisation
Notre Fer doit être pris pendant le déjeuner.
Combien de gélules de notre Fer
- 1 gélule par jour.
Durée d’une prise
- Notre Fer doit être pris au besoin, selon les recommandations de votre professionnel de santé.
Comment prendre notre Fer
- Prendre 1 gélule par jour avec un grand verre d’eau.
- Peut-on ouvrir ses gélules ? Oui, mais il existe cependant un risque que le produit perde en efficacité.
Durée d’une boîte
- La boîte de notre Fer dure 1 mois, à raison d’1 gélule par jour.
Précautions d’emploi
- Complément alimentaire à base de fer, à utiliser en complément d'une alimentation saine et équilibrée.
- Ne pas dépasser la dose journalière indiquée.
- Convient aux femmes enceintes et allaitantes (les femmes enceintes et allaitantes sont invitées à prendre l’avis d’un médecin avant toute supplémentation).
- Non destiné aux enfants.
- Déconseillé aux personnes souffrant de maladies ayant pour conséquence une accumulation anormale de fer (hémochromatose, polyglobulie).
- Le Fer doit être pris en contrôlant votre taux de ferritine.
Conditions de conservation
- À conserver dans un endroit sec et à l'abri de la lumière et de la chaleur.
- À tenir hors de portée des enfants.
Tout savoir sur le Fer
La carence en fer : aspects biologiques et données chiffrées
Le fer est l’élément chimique (symbole Fe) de numéro atomique 26. C’est l'oligo-élément le plus abondant, et donc le plus étudié du corps humain. Un oligo-élément est un minéral (fer mais aussi zinc, sélénium…) dont le besoin nutritionnel est inférieur à la catégorie des minéraux (magnésium, calcium…). En effet, en plus d’être relativement courantes, les carences en fer sont associées à des mécanismes d’absorption et de régulation extrêmement complexes. Or une carence en fer, si elle se transforme en anémie, peut avoir des conséquences graves pour la santé.
Définition de la carence en fer
Le risque de carence potentielle apparaît essentiellement lorsque les besoins de l’organisme sont augmentés (pour compenser par exemple des pertes plus importantes), et que les apports ne sont pas ajustés en conséquence.
Les premiers stades d’une carence en fer ne sont pas nécessairement associés à une anémie, même si cela s’avère fréquent. [1,2]
La carence en fer sans anémie (appelée carence martiale) est caractérisée par une diminution de la ferritine, protéine de stockage cellulaire du fer dans les organes et présente en plus faible quantité dans le sang. La ferritine est le marqueur direct des réserves en fer de l'organisme et son dosage sanguin permet de détecter une carence.
La diminution de la ferritine (carence en fer non anémique : <15–30 μg/l identifiable via analyse sanguine) est très précoce, elle survient avant même l’installation de l’anémie (et lorsque l’anémie s’installe, la ferritine s’écroule).
L’anémie est caractérisée par une diminution de l’hémoglobine (protéine des globules rouges de transport de l’oxygène), et peut être causée par une carence en fer ou d’autres facteurs. Le dosage sanguin de l’hémoglobine permet de la diagnostiquer (<130g/l pour les hommes et <120g/l pour les femmes).
L’anémie causée par une carence en fer est donc associée à une ferritine basse, elle est appelée anémie ferriprive.
Il est important de noter que l’anémie peut avoir d’autres origines qu’une carence en fer :
- une carence en folates (vitamine B9),
- une carence en vitamine B12.
Notons que la carence en fer sans anémie est un état latent de l’anémie ferriprive.

Adapté de [2]
Conséquences pour la santé
L’anémie par carence en fer entraîne différents symptômes comme la fatigue, la pâleur du teint et un essoufflement plus prononcé à l’effort. Les symptômes de la seule carence en fer (sans anémie) sont quant à eux moins bien établis, mais cet état affecterait également le bien-être général [2].
Lors de la grossesse, le statut nutritionnel de la mère est crucial et les périodes pré, péri et post-natales sont des fenêtres de programmation de la santé de l’enfant. Un statut en fer adéquat durant la grossesse va permettre une maturation du cerveau et un développement normal du nouveau-né puis de l’enfant [3]. Il apparaît donc important de surveiller les apports en fer des femmes enceintes et, plus tard, des jeunes enfants.
Données de prévalence
Une grande analyse a été réalisée entre 1993 et 2005 par l’Organisation Mondiale de la Santé (OMS) sur 192 pays afin de déterminer la prévalence de l’anémie. Ces travaux ont évalué à 1,62 milliards le nombre de personnes touchées par l’anémie, soit 24,8% de la population mondiale. Tous les pays ne sont évidemment pas touchés de la même manière.
Si on regarde l’Europe, la prévalence de l’anémie chez les femmes enceintes était de 25,1% contre 19% pour les autres femmes [4]. La prévalence chez les jeunes enfants (0-5 ans) était de 21,7%.
L’OMS a par ailleurs évalué le pourcentage d’anémies pouvant être concernées par une supplémentation (par des compléments alimentaires de fer notamment) en fer (anémie qui tirerait donc son origine de la carence en fer). En Europe, l’organisme donne les chiffres suivants :
- 54% des anémies chez l’enfant (6 mois à 5 ans) pourraient être corrigées par une supplémentation en fer,
- 55% des anémies chez la femme menstruée ou en âge de procréer (15-49 ans),
- et 62% des anémies chez la femme enceinte (15-49 ans).
Tous pays confondus, les travaux ont établi que 50% des anémies chez les femmes (menstruées, en âge de procréer, enceintes) résulteraient d’une carence en fer.
Des données spécifiques à la population française ont été publiées en 2001 [5] :
- Chez les femmes menstruées, la prévalence du déficit en fer était entre 8,1 et 23% avec 1,3 à 4,4% associés à une anémie,
- Chez les femmes enceintes, la prévalence du déficit en fer était entre 54 et 77% avec 9 à 30% associés à une anémie,
- Chez les enfants de moins de 2 ans, la prévalence du déficit en fer était de 29,2% avec 4,2% associés à une anémie,
- Chez les enfants de moins de 2 à 6 ans, la prévalence du déficit en fer était de 13,6% avec 2% associés à une anémie,
- Chez les hommes adultes et les sujets âgés, la prévalence est faible.
En résumé, bien que l’anémie ne soit pas forcément due à une carence en fer, les données suggèrent une forte probabilité que celle-ci en soit la cause. Il apparaît donc nécessaire de suivre le statut en fer de la population, notamment en France, avec une attention particulière chez les personnes à risque de carence, et donc aussi à risque d’anémie (essentiellement les femmes enceintes ou en âge de procréer et les jeunes enfants).
Le fer de notre organisme et de notre alimentation
Les deux formes de fer dans l'organisme [6]
Deux formes de cations du fer existent : le fer ferreux Fe2+ et le fer ferrique Fe3+. La majorité du fer de l'organisme (70%) est sous forme dite “héminique” (ferreux, Fe2+ contenu dans l’hème), le reste étant sous forme “non héminique” (ferrique, Fe3+, forme de transport et de réserve) :
- Le Fe2+ (fer ferreux) : Il est présent à plusieurs niveaux dans l'organisme et entre dans la composition de :
- L'hémoglobine : 2,4g soit 60% du fer total. L’hémoglobine est la protéine des globules rouges liée en son centre par un co-facteur appelé l’hème contenant un atome de fer. Cette structure est capable de recevoir une molécule d’oxygène et de la transporter. En entrant dans la composition de l’hémoglobine, le fer est donc indispensable à la formation des globules rouges (= érythrocytes), phénomène d’érythropoïèse, ainsi qu’au transport de l’oxygène.
- La myoglobine : 0,2g soit 5% du fer total. La myoglobine est la protéine du muscle permettant le stockage de l’oxygène.
- Plusieurs enzymes de la respiration cellulaire (cytochromes, oxydases, peroxydase, catalases, enzymes du cycle de Krebs) et la synthèse de l’ADN : 0,01g soit 0,3% du fer total. Le Fe2+ entre dans la composition des mitochondries (cytochrome C) et participe au renouvellement cellulaire, à la synthèse d’hormones et de neurotransmetteurs.
- Le Fe3+ (fer ferrique) : Au sein de l’organisme, il est utilisé pour :
- Les réserves de fer : 1,4g soit 35% du fer total est inclus dans la ferritine (majoritairement ; protéine de stockage du fer),
- Le fer de transport : 0,005g est lié à la transferrine (protéine chargée du transport du fer dans le plasma).
Le fer alimentaire
Fe2+ est la forme que l’on retrouve dans les tissus animaux (comme dans la viande et le poisson) tandis que la forme Fe3+ est retrouvée dans les céréales, les légumineuses (les végétaux) et les œufs. Il existe donc deux types d’apport alimentaire en fer, en fonction de la forme, et des grandes catégories d’aliments dans lesquels on les retrouve (tableau ci-après). Entre ces deux formes l’absorption par l’organisme ne sera aussi pas la même :
- Le fer Fe2+ (héminique, d’origine animale) est la forme la mieux absorbée par l’organisme (de 15 à 20%),
- Le fer non-héminique (essentiellement d’origine végétale) est la forme la moins bien absorbée par l’organisme, de 3 à 5%
Aliment Fer (mg de/100g) - valeur moyenne Origine animale Boudin noir (cuit) 16,1 Abats (cuits) 6,5 Moules (cuites) 4,0 Viande rouge (cuite) 2,8 Oeufs (cuits) 1,8 Charcuterie 1,6 Viande blanche (cuite) 0,8 Poisson (cuit) 0,7 Origine végétale Graines de sésame 14,6 Epinards (cuits) 2,1 Légumineuses (cuites) 1,6 Légumes (cuits) 0,5 Riz complet (cuit) 0,3 Avocat (pulpe) 0,3 Riz blanc (cuit) 0 *La composition nutritionnelle des aliments est consultable sur le site de l'ANSES, Agence nationale de sécurité sanitaire de l'alimentation, l'environnement et du travail.
- Le Fe2+ (fer ferreux) : Il est présent à plusieurs niveaux dans l'organisme et entre dans la composition de :
Le métabolisme du fer
Le cycle général du fer dans l’organisme [7–9]
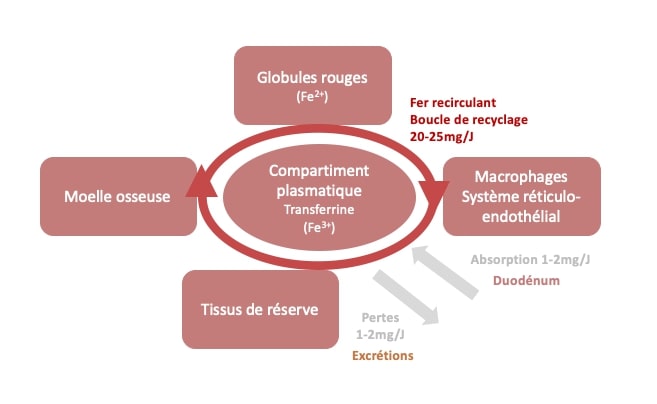
Au sein de l'organisme existe un système bien rodé autour du fer. Si la capacité d’absorption au niveau entérocytaire (cellules de la paroi de l’intestin grêle) est de 1 à 2mg par jour, les pertes sont d'environ du même ordre, 1 à 2mg par jour, en raison de pertes cellulaires (exemple: cellules digestives, de la peau et des phanères) et de diverses sécrétions (sueur, urine, bile ou lait maternel). Le seul mécanisme de régulation des taux de fer dans l’organisme se situe au niveau de l'absorption. En réalité, les apports et pertes sont deux mécanismes quasiment indépendants, et il est possible d’accumuler “trop de fer” si les apports sont trop importants par rapport aux pertes.
Le fer est également soumis à un système de recyclage, pool “recirculant” de 20 -25mg par jour, entre la synthèse des globules rouges dans la moelle osseuse et leur destruction normale (phagocytose) par le système réticulo-endothélial (ensemble de cellules immunitaires impliquées dans l’épuration de l’organisme).

L’absorption du fer alimentaire dans l’organisme [9,10]
En situation physiologique, l’absorption intestinale est la seule voie d’entrée du fer. Après une étape de solubilisation dans l’estomac, le niveau d'absorption est maximal au tout début de l’intestin grêle (cellules entérocytaires matures).
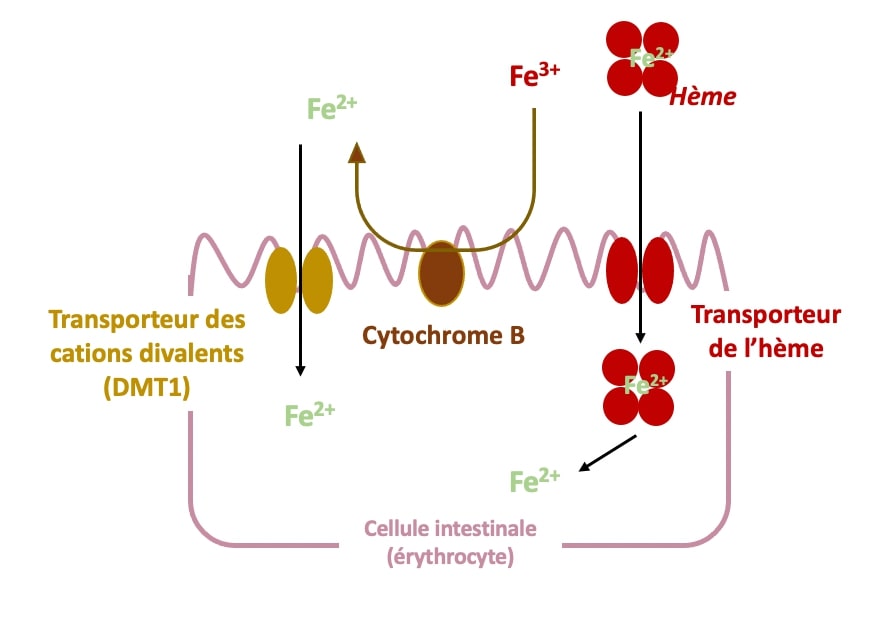
- Fe2+(la forme la mieux absorbée, 15-20% du total présent dans l’intestin) : Quand il est héminique (dans l’hème), il est directement absorbé par la muqueuse intestinale via un transporteur spécifique de l’hème.
- Fe3+ (non-héminique, la forme la moins bien absorbée 3-5%) : Quel que soit l’apport, via les aliments ou la Nutra sous forme de sels ferriques, il doit d’abord être réduit par le cytochrome B intestinal (DCYTB) en Fe2+ qui peut alors être pris en charge par le DMT1.
L’absorption du fer nutraceutique dans l’organisme
Il n’existe pas que du fer alimentaire. Lorsque les déficits existent, on peut passer par des sel nutraceutiques.
- Fe2+ : Lorsqu’il est sous forme Fe2+ non-héminique, le fer est absorbé directement via DMT1 et présente donc une absorption moindre par rapport à sa forme héminique.
- Fe3+ : Il existe aussi certaine forme de Fe3+ présent dans certains sels comme le Hydroxyde ferrique polymaltose. Comme le Fe3+ alimentaire, son absorption est moins bonne que le Fe2+ héminique.

En conclusion on retrouve :
Caractéristique Héminique Non-héminique Forme du fer Fe2+ Fe2+ Fe3+ Dans l'organisme Oui Non Oui Origine Animale Sels ferreux (nutra) Essentiellement végétale ou Sels ferriques (nutra) Absorption Directe par le transporteur érythrocytaire de l’hème Directe par le transporteur érythrocytaire DMT1 Réduction en Fe2+via le DCYTB érythrocytaire et transport via DMT1 La régulation de l’absorption dans l’organisme [11,12]
La régulation des stocks de fer est hormonale et se joue essentiellement au niveau de l’absorption. Un petit peptide hormonal synthétisé par le foie joue un rôle crucial dans le contrôle de l'absorption du fer : l’hepcidine.
En fixant la ferroportine, transporteur du fer de l’intérieur des entérocytes (cellules intestinales) vers la circulation sanguine, l’hepcidine entraîne sa dégradation. En résumé, l’hepcidine agit en diminuant l’absorption intestinale du fer alimentaire ainsi que le recyclage du fer des globules rouges par les macrophages. L’expression de l’hepcidine est réglée en fonction de différents stimuli :
- Lorsque l’organisme en a besoin, l’hepcidine diminue et le fer est totalement capté par les entérocytes pour rejoindre rapidement la circulation sanguine (de même que le fer issu des macrophages). En bref, une concentration plasmatique faible d’hepcidine est donc associée à des mouvements importants du fer aboutissant à une élévation du taux de fer de l’organisme.
- En cas d’apports alimentaires élevés en fer et d’une inflammation (et/ou infection), l’hepcidine est augmentée et le fer reste au sein des entérocytes et des macrophages. En bref, une concentration augmentée d’hepcidine entraîne un blocage des mouvements de fer aboutissant à la limitation de l’élévation des taux de fer de l'organisme.
Par exemple, en cas de perte importante de sang, l’hepcidine est réduite, afin de permettre une absorption maximale de Fer, qui permet une activation de l’érythropoïèse (synthèse des globules rouges).
Biodisponibilité du fer [13,14]
Le fer dans l’hème est la forme ayant la meilleure biodisponibilité (15 à 20%) avec le Fe2+ sous forme ionique (absorption très variable selon la formule ou la source).
Le fer végétal étant sous forme de Fe3+, il doit être réduit pour pouvoir être absorbé. De plus, dans les végétaux, certains composés complexent le fer (comme les phytates) l’empêchant ainsi d’être réduit et assimilé. Au total, le fer végétal affiche donc une absorption particulièrement faible de 3% à 5%.
On sait par exemple que, la consommation de thé inhibe l’absorption du fer dû à la présence de polyphénols capables de complexer le fer : les tannins. D’autres polyphénols des légumes et des céréales pourraient être impliqués mais les données ne sont pas encore très claires.
D’autres composés sont, quant à eux, facilitateurs de l’absorption du fer. La vitamine C (acide ascorbique) a démontré qu’elle était capable de faciliter la réduction du fer ferrique en fer ferreux ainsi que de chélater le fer (fer rendu soluble).
Enfin, certains métaux lourds pourraient être en compétition avec les mécanismes d'absorption du fer. Le plomb est un exemple de compétiteur du fer, mais la prévalence reste faible chez les enfants en bas-âge, population la plus vulnérable.
Apports et besoins en fer
Aspects généraux des besoins [15]
Le fer répond à un mécanisme d’équilibre. Les apports doivent strictement compenser les pertes. Dans le cadre d’un déséquilibre, le risque de déficience (voire de carence) ou de surcharge (possiblement pathologique) peut survenir. En additionnant la quantité de fer contenu dans l'organisme et pour chaque compartiment, on obtient un total de 4g (un peu moins pour les femmes, plus proche de 3g) de fer au total (cf paragraphe : les deux formes de fer). Les apports alimentaires tournent autour de 10 à 15mg par jour mais la capacité d'absorption intestinale est de 1 à 2mg par jour.
Le fer étant stocké dans l’organisme, les apports nutritionnels de référence ont donc été élaborés de manière à assurer les réserves. En 2016, les recommandations ont été revues à 11 mg/j pour :
- L’homme,
- La femme ayant des pertes menstruelles faibles ou normales (80% de la population féminine non ménopausée),
- La femme ménopausée.
Les situations physiologiques spécifiques [15]
Le fer alimentaire sert à combler les pertes mais aussi à subvenir à l’augmentation des besoins dans certaines situations physiologiques (adaptation de l’absorption). Parmi ces situations sujettes aux déficiences en fer par demande croissante, on distingue (données EFSA pour les apports de références : https://www.efsa.europa.eu/fr/topics/topic/dietary-reference-values) :
- Les femmes avec des pertes menstruelles élevées. Les apports recommandés passent alors de 11mg/j à 16mg/j.
- Les femmes enceintes et allaitantes. Les apports recommandés passent alors de 11mg/j à 16mg/j.
- Les nourrissons de 7-11 mois. Les apports recommandés sont déjà de 11mg/j.
- Les adolescents et notamment les adolescentes (12-17 ans). Les apports recommandés sont de 13mg/j.
Les situations non-physiologiques de vigilance
Tous les cas de figure de changement du besoin ne sont pas forcément référencés par les instances et autorités de santé. On peut notamment dégager des modes de vie susceptibles d’induire des besoins plus importants.
- Les régimes alimentaires pauvres en viande et/ou poisson sont pauvres en fer et augmentent le risque de déficience en fer. Ces régimes sont notamment représentés par des apports en fer non héminique dont les sources contiennent elles-mêmes des facteurs limitant l’absorption du fer dont les fameux phytates, très présents dans le soja par exemple (cf partie : Biodisponibilité du fer) [16].
- Les femmes végétariennes et vegans, versus les non-végétariennes, ont une prévalence plus élevée de risque d’anémie par carence en fer [17].
Un autre cas de figure peut-être soulevé. Dans le cadre d’entraînements sportifs intenses, il est d’autant plus important de vérifier le statut en fer et les apports chez les femmes. Bien que les données ne mettent pas toutes en évidence une relation établie entre entraînement intensif et carence en fer (ou besoin de supplémentation) [18], la surveillance du statut et des apports en fer est largement encouragée afin d'optimiser la performance [19].
Etat des apports en fer
En France, l’étude INCA III (Étude Individuelle Nationale des Consommations Alimentaires) a évalué les apports en fer de différentes tranches d’âges (0-10 ans, 11-17 ans et 18-79 ans) [20] :
Tranche d’âges Apport en fer, mg/j 0-10 ans, moyenne globale
Focus 0-11 mois :
8,2
6,6
0-10 ans, moyenne garçons 8,7 0-10 ans, moyenne filles 7,7 11-17 ans, moyenne globale 9,8 11-17 ans, moyenne garçons 10,7 11-17 ans, moyenne filles 8,9 18-79 ans, moyenne globale 10,5 18-79 ans, moyenne hommes 12,2 18-79 ans, moyenne femmes 8,9 Les résultats de ces travaux montrent que la plupart des tranches d’âge et catégories ont des apports en-deçà des recommandations nutritionnelles.
En 2019, une revue à l’échelle européenne sur les apports spécifiques en fer des femmes en âge de procréer a montré que, dans une très large majorité des pays, les apports en fer sont inférieurs aux 11mg/jour recommandés [21].
La supplémentation en fer
La cible majeure : les femmes enceintes [2,22,23]
La supplémentation en fer s’adresse particulièrement aux femmes enceintes afin de prévenir l’anémie maternelle et les complications directes liées au développement du fœtus. Durant la grossesse, les besoins en fer augmentent fortement en réponse à une expansion de 30% de la masse corporelle en globules rouges.
Les apports en fer sont une préoccupation de santé publique majeure, référencée par l’Organisation Mondiale de la Santé (OMS). Pour assurer ces besoins accrus durant la grossesse, l’apport en fer recommandé est d’environ 30mg/jour, dose presque 2 fois supérieure aux besoins élémentaires et pouvant causer un inconfort digestif. Des formules de compléments alimentaires de fer à libération lente permettraient de l’éviter mais elles ne seraient pas aussi efficaces à réellement couvrir les besoins. Par ailleurs, cette dose ne serait justifiée que pour une carence martiale observée avant et pendant la grossesse.
Il semblerait que par prévention et pour veiller à ne pas basculer dans la carence, des formulations avec des doses bien plus faibles et optimisant l'absorption du fer soient plus adaptées.
Les formes de fer en nutraceutiques [24,25]
Hors du contexte alimentaire et de l’organisme, le lien ou non du fer avec l’hème n’a plus de sens. Dans la littérature, plusieurs formulations de fer sont référencées à base de fer ferreux (Fe2+) ou de fer ferrique (Fe3+ ) (sous forme de sels) :
- Gluconate ferreux (Fe2+),
- Citrate ferreux (Fe2+),
- Sulphate ferreux (Fe2+),
- Fumarate ferreux (Fe2+),
- Bisglycinate de fer (Fe2+),
- Succinylate de protéine de fer (Fe3+ ),
- Hydroxyde ferrique polymaltose (Fe3+ ).
Les formes de sels ferreux (Fe2+) sont mieux absorbées, donc plus biodisponibles. En Nutraceutique, on retrouve de moins en moins certains sels (sulfate) par rapport à des formes plus récentes (bisglycinate). Selon la forme de sel, la teneur en fer élément n’est pas la même. C’est le fumarate ferreux qui contient le plus de fer élément : 33%, comparativement au bisglycinate à 20% ou encore au gluconate ferreux à 12%. A noter que c’est la solubilité en milieu acide (estomac) qui entraîne la libération rapide des ions Fe2+ au début de l’intestin grêle et qui détermine la qualité de l’absorption du fer. C’est en cela que le bisglycinate de fer d’Albion Minerals se distingue.
Penser d’abord à l’absorption
Afin d’éviter les quantités élevées en fer et leurs effets secondaires indésirables, il est possible de se pencher spécifiquement sur l’optimisation de l’absorption du fer.
L’augmentation de l'absorption du fer par la vitamine C est documentée depuis plus de 40 ans. Bien que les données ne se corroborent pas toujours, elles mettent en évidence un intérêt de la vitamine C dans l’optimisation de l’absorption du fer non-héminique [26]. D’une part, cette optimisation dépendrait du statut en fer de l’individu (ferritine plasmatique). Plus ce statut serait bas, plus efficace serait la vitamine C sur l’absorption du fer [27]. D’autre part, le ratio vitamine C/fer serait intéressant. Plus le régime alimentaire serait riche en inhibiteurs de l’absorption du fer (comme les phytates), plus l’absorption du fer serait optimisée par un ratio vitamine C/fer augmenté [28]. Si la vitamine C est l’un des facteurs les plus connus sur l’amélioration de l'absorption du fer, d’autres travaux sont encore nécessaires pour mieux comprendre son niveau d’intérêt.
Aussi, la compétition avec l'absorption du zinc (Zn2+) et du calcium (Ca2+) semble uniquement valable dans des conditions d’apports très élevés. C’est-à-dire dans un cas de supplémentation importante et simultanée par exemple de ces 3 minéraux [29].
Enfin, de façon intéressante, une méta-analyse a démontré l’effet de souches lactiques sur l’amélioration de l’absorption du fer non-héminique et du statut en fer dans plusieurs études cliniques [30]. Par hypothèse, certaines souches spécifiques favoriseraient les mécanismes d’absorption du fer non-héminique (par DCYTB (réduction du Fe3+ en Fe2+) et DMT1 (entrée dans la cellule)) en capturant le fer au niveau duodénal [31].
La formule Nutri&Co : Le Fer et sa Souche Lactique
Bien plus qu’un simple complément alimentaire de fer, notre Fer et sa Souche Lactique réunit 4 éléments :
- du fer apporté par du bisglycinate de fer breveté, à hauteur de 14mg, “en soutien” aux apports alimentaires, et jouant un rôle dans le processus de division cellulaire,
- une souche lactique : Lactobacillus plantarum 299vⓇ ,
- de la vitamine B9 apportée sous forme de folate réduit : 5-Méthyltétrahydrofolate* (5-MTHF, le QuatrefolicⓇ), contribuant à la croissance des tissus maternels,
- de la vitamine C (acide ascorbique) augmentant l’absorption du fer.
*La prise en supplément de 5-Méthyltétrahydrofolate (5-MTHF), forme bioactive, permet d’obtenir une biodisponibilité élevée de vitamine B9. En effet, la forme 5-MTHF subit moins de transformations enzymatiques pour devenir active en comparaison avec l’acide folique [32].
Trois études cliniques ont été réalisées sur la formule que nous avons sélectionnée.
Chez des femmes en âge de procréer et chez des sportifs d’endurance, les résultats montrent que l’absorption du fer est significativement plus élevée (différence de 47% et de 23% respectivement) dans les groupes recevant la souche, comparativement à ceux recevant la formule sans Lactobacillus plantarum 299vⓇ [33,34].
Enfin, dans une étude réalisée sur 326 femmes enceintes, les analyses montrent que la prise de la formule avec Lactobacillus plantarum 299vⓇ a significativement limité la baisse (versus placebo) des marqueurs sanguins liés au fer de ces femmes (ferritine et hémoglobine au cours de la grossesse; mesures à 25, 28 et 35 semaines de grossesse). La ferritine a baissé de 46,2µg/L dans le groupe ayant utilisé la formule, alors qu’elle a baissé de 52,7µg/L dans le groupe placebo à 35 semaines. Enfin, l’hémoglobine avait davantage diminué dans le groupe placebo (-13,7g/L) par rapport au groupe prenant la formule avec souche (-9,1g/L) [35].
Autrement dit, même si les marqueurs sanguins baissent logiquement pendant la grossesse, notre formule pourrait diminuer significativement cette baisse de :
- 13% pour la ferritine,
- 34% pour l’hémoglobine.
Références scientifiques
1. HAS RAPPORT D’EVALUATION - CHOIX DES EXAMENS DU METABOLISME DU FER EN CAS DE SUSPICION DE CARENCE EN FER; 2011; p. 82;.
2. Pasricha, S.-R.; Tye-Din, J.; Muckenthaler, M.U.; Swinkels, D.W. Iron Deficiency. Seminar 2020, 1–16.
3. Black, M.M.; Quigg, A.M.; Hurley, K.M.; Pepper, M.R. Iron Deficiency and Iron-Deficiency Anemia in the First Two Years of Life: Strategies to Prevent Loss of Developmental Potential: Nutrition Reviews©, Vol. 66, No. S1. Nutr. Rev. 2011, 69, S64–S70, doi:10.1111/j.1753-4887.2011.00435.x.
4. De Benoist, B.; World Health Organization; Centers for Disease Control and Prevention (U.S.) Worldwide Prevalence of Anaemia 1993-2005 of: WHO Global Database of Anaemia; World Health Organization: Geneva, 2008; ISBN 978-92-4-159665-7.
5. Hercberg, S.; Preziosi, P.; Galan, P. Iron Deficiency in Europe. Public Health Nutr. 2001, 4, 537–545, doi:10.1079/PHN2001139.
6. Dassonneville, M. Métabolisme du fer et anémie par carence martiale, 2015.
7. Anderson, G.J.; Frazer, D.M.; McLaren, G.D. Iron Absorption and Metabolism. 2009, 7.
8. Winter, W.E.; Bazydlo, L.A.L.; Harris, N.S. The Molecular Biology of Human Iron Metabolism. 2014, 11.
9. Yiannikourides, A.; Latunde-Dada, G.O. A Short Review of Iron Metabolism and Pathophysiology of Iron Disorders. 2019, 15.
10. Silva, B.; Faustino, P. An Overview of Molecular Basis of Iron Metabolism Regulation and the Associated Pathologies. Biochim. Biophys. Acta BBA - Mol. Basis Dis. 2015, 1852, 1347–1359, doi:10.1016/j.bbadis.2015.03.011.
11. Nicolas, G. L’hepcidine, le chef d’orchestre de l’homéostasie du fer. Diabète Obésité 2009, 94–98.
12. Wallace, D.F. The Regulation of Iron Absorption and Homeostasis. 2016, 37, 12.
13. Hurrell, R.; Egli, I. Iron Bioavailability and Dietary Reference Values. Am. J. Clin. Nutr. 2010, 91, 1461S-1467S, doi:10.3945/ajcn.2010.28674F.
14. Abbaspour, N.; Hurrell, R.; Kelishadi, R. Review on Iron and Its Importance for Human Health. J. Res. Med. Sci. 2014, 12.
15. EFSA Scientific Opinion on Dietary Refrence Values for Iron; 2015; p. 115;.
16. Phillips, F. Vegetarian Nutrition. Nutr. Bull. 2005, 30, 132–167, doi:10.1111/j.1467-3010.2005.00467.x.
17. Pawlak, R.; Berger, J.; Hines, I. Iron Status of Vegetarian Adults: A Review of Literature. Am. J. Lifestyle Med. 2018, 12, 486–498, doi:10.1177/1559827616682933.
18. Houston, B.L.; Hurrie, D.; Graham, J.; Perija, B.; Rimmer, E.; Rabbani, R.; Bernstein, C.N.; Turgeon, A.F.; Fergusson, D.A.; Houston, D.S.; et al. Efficacy of Iron Supplementation on Fatigue and Physical Capacity in Non- Anaemic Iron-Deficient Adults: A Systematic Review of Randomised Controlled Trials. BMJ Open 2017, 9.
19. Alaunyte, I. Iron and the Female Athlete: A Review of Dietary Treatment Methods for Improving Iron Status and Exercise Performance. 2015, 7.
20. ANSES Etude Individuelle Nationale Des Consommations Alimentaires 3 (INCA 3). Avis de l’ANSES. Rapport d’expertise Collective; 2017; p. 566;.
21. Milman, N.T. Dietary Iron Intake in Women of Reproductive Age in Europe: A Review of 49 Studies from 29 Countries in the Period 1993–2015. J. Nutr. Metab. 2019, 13.
22. ANSES AVIS de l’Agence Française de Sécurité Sanitaire Des Aliments Relatif à l’évaluation Des Justificatifs Concernant Le Dépassement Des Doses Maximales Admises En Folates, Vitamine D et En Fer Dans Un Complément Alimentaire Destiné Aux Femmes En Période Périconceptionnelle et Aux Femmes Enceintes.; 2007; p. 4;.
23. Petry, N.; Olofin, I.; Hurrell, R.; Boy, E.; Wirth, J.; Moursi, M.; Donahue Angel, M.; Rohner, F. The Proportion of Anemia Associated with Iron Deficiency in Low, Medium, and High Human Development Index Countries: A Systematic Analysis of National Surveys. Nutrients 2016, 8, 693, doi:10.3390/nu8110693.
24. Santiago, P. Ferrous versus Ferric Oral Iron Formulations for the Treatment of Iron Deficiency: A Clinical Overview. Sci. World J. 2011, 5.
25. Manoguerra, A.S.; Erdman, A.R.; Booze, L.L.; Wax, P.M.; Scharman, E.J.; Woolf, A.D.; Chyka, A.; Keyes, D.C.; Olson, K.R.; Caravati, E.M. Iron Ingestion: An Evidence-Based Consensus Guideline for Out-of-Hospital Management. Clin. Toxicol. 2005, 43, 553–570.
26. Heffernan, A.; Evans, C.; Holmes, M.; Moore, J.B. The Regulation of Dietary Iron Bioavailability by Vitamin C: A Systematic Review and Meta-Analysis. Proc. Nutr. Soc. 2017, 76, E182, doi:10.1017/S0029665117003445.
27. Collings, R.; Harvey, L.J.; Hooper, L.; Hurst, R.; Brown, T.J.; Ansett, J.; King, M.; Fairweather-Tait, S.J. The Absorption of Iron from Whole Diets: A Systematic Review1–4. Am J Clin Nutr 2013, 98, 65–81.
28. Teucher; Olivares; Cori Enhancers of Iron Absorption: Ascorbic Acid and Other Organic Acids. Int. J. Vitam. Nutr. Res. 2004, 74, 403–419, doi:10.1024/0300-9831.74.6.403.
29. Scheers, N. Regulatory Effects of Cu, Zn, and Ca on Fe Absorption: The Intricate Play between Nutrient Transporters. nutrients 2013, 14.
30. Vonderheid, S.C.; Tussing-Humphreys, L.; Park, C.; Pauls, H.; OjiNjideka Hemphill, N.; LaBomascus, B.; McLeod, A.; Koenig, M.D. A Systematic Review and Meta-Analysis on the Effects of Probiotic Species on Iron Absorption and Iron Status. Nutrients 2019, 11, 2938, doi:10.3390/nu11122938.
31. Sandberg, A.-S.; Önning, G.; Engström, N.; Scheers, N. Iron Supplements Containing Lactobacillus Plantarum 299v Increase Ferric Iron and Up-Regulate the Ferric Reductase DCYTB in Human Caco-2/HT29 MTX Co-Cultures. Nutrients 2018, 10, 1949, doi:10.3390/nu10121949.
32. Pietrzik, K.; Bailey, L.; Shane, B. Folic Acid and L-5-Methyltetrahydrofolate: Comparison of Clinical Pharmacokinetics and Pharmacodynamics. Clin. Pharmacokinet. 2010, 49, 535–548, doi:10.2165/11532990-000000000-00000.
33. Hoppe, M.; Önning, G.; Berggren, A.; Hulthén, L. Probiotic Strain Lactobacillus Plantarum 299v Increases Iron Absorption from an Iron-Supplemented Fruit Drink: A Double-Isotope Cross-over Single-Blind Study in Women of Reproductive Age. Br. J. Nutr. 2015, 114, 1195–1202.
34. Hoppe, M. Freeze-Dried Lactobacillus Plantarum 299v Increases Iron Absorption in Young Females— Double Isotope Sequential Single-Blind Studies in Menstruating Women. PLoS ONE 2017, 12, 15.
35. Axling, U.; Önning, G.; Martinsson Niskanen, T.; Larsson, N.; Hansson, S.R.; Hulthén, L. The Effect of Lactiplantibacillus Plantarum 299v Together with a Low Dose of Iron on Iron Status in Healthy Pregnant Women: A Randomized Clinical Trial. Acta Obstet. Gynecol. Scand. 2021, aogs.14153, doi:10.1111/aogs.14153.

Une infographie ludique pour enfin tout comprendre sur le Fer Bisglycinate
Voir l'infographie
Combien de gélules pour moi ?
Découvrez en quelques minutes votre posologie personnalisée.
Faire le questionnaireLes avis de nos clients sur le Fer Bisglycinate
4,6(139)Amina A.
16/05/2026Très efficace, j ai utilisé le fer bisglycinate de nutri&co pendant deux mois et je suis devenu plus active , j’ai moins de fatigue et beaucoup d’énergie.
Sandra B.
14/05/2026Je l’ai débuté il y a peu mais on ressent bien que c’est différent du tardyferon. Pas de douleurs abdominal ou autres. Pour ma part je le tolère bien mieux. Maintenant on va attendre plusieurs semaines car je suis très basse dans ma ferritine
Rhizlane H.
09/05/2026Mon fer remonte à la fin du traitement !
Corinne J.
06/05/2026Je commence tout juste .j'ai une ferritine basse. Je prends 1 gelule par jour , loin des repas , avec une fruit riche en vitamines C , pour une absorption optimal . Je mettais un avis dans 2 mois.
Fanny R.
05/05/2026Très bon complément en fer ! Je recommande !


Vos questions sur le Fer
Nos experts répondent à toutes vos questions.
Le fer est-il pro-oxydant comme on le voit dans certains articles sur le net ?
On parle d’effet “pro-oxydant” pour une molécule qui génère un stress oxydatif, ou des espèces réactives de l’oxygène (ROS ou radicaux libres).
Le fer peut effectivement jouer ce rôle-là dans des situations bien particulières :
- un excès de fer qui s'accumule dans les cellules et qui cause une toxicité,
- par oxydation de fer II en fer III qui génère des radicaux libres.
Comme souvent, c’est donc la dose qui fait le poison et le fer peut devenir pro-oxydant si les apports sont trop importants par rapport aux besoins physiologiques. C’est aussi pour éviter ce type de problème que notre Fer a été développé.
Combien de temps est nécessaire pour faire remonter mon taux de fer avec une supplémentation ?
Suivant le manque observé (anémie, carence martiale ou simple stock diminué), le temps de restauration d’un bon taux de ferritine sera plus ou moins long. Dans le cas d’un déficit léger, le taux de ferritine retrouve un niveau normal en quelques jours. La supplémentation devra bien entendu être encadrée par un médecin de façon à suivre les marqueurs sanguins et leur évolution positive (hémoglobine si anémie, et ferritine si uniquement carence).

Quels sont les signes d'un manque de fer ? Est-il possible de savoir si j’en manque?
Oui. Le dosage d’un marqueur particulier est possible : la ferritine. Cette dernière est le reflet direct des réserves en fer. En dessous de 15-30μg/l, elle indique une carence martiale en fer. Bien entendu, ces valeurs sont ensuite à confirmer avec votre médecin pour ensuite envisager une supplémentation adaptée.
Je suis thalassémique est-ce que je peux prendre votre formule ?
Non. L'ensemble des maladies héréditaires dites thalassémies résultent d'anomalies au niveau de l'hémoglobine des globules rouges et non de carence en fer. Aussi, notre Fer et sa souche lactique n’apportera pas une réponse adaptée.
La gélule de fer a-t-elle un goût métallique ?
Non. A contrario des comprimés ou des solutions dont le goût métallique est caractéristique, le fer en gélules présente l’avantage de ne pas avoir de goût.
Peut-on associer apport en Fer et prise de spiruline ?
Oui. Il est tout à fait possible de combiner notre Fer avec notre Spiruline. Au regard de la teneur très faible en fer dans notre Spiruline (7% des AR par portion, 6 comprimés), le fer sera majoritairement apporté par notre Fer et sa Souche Lactique.
Dois-je prendre cette formule en même temps qu'une alimentation riche en fer ?
Non. Notre Fer est une supplémentation en réponse à des besoins soit parfois difficiles à couvrir, soit accrus dans certaines situations (femmes enceintes, femmes aux pertes menstruelles importantes, femmes au désir de grossesse). Toute supplémentation en fer doit être justifiée soit par un état déficitaire en fer (idéalement avéré par une prise de sang via dosage de la ferritine), soit par un état physiologique qui l'exige comme les cas cités ci-dessus.
Est-ce bon de faire une cure de fer ?
Faire une cure de fer est nécessaire seulement si vous en manquez ou que vous souffrez d’anémie. Parlez-en avec votre médecin.
Quel est le meilleur complément alimentaire en fer ?
Un bon complément en fer doit inclure une forme bien absorbée et qui ne provoque pas de troubles digestifs, comme le bisglycinate de fer. De plus, d’autres actifs, comme la vitamine C et notre probiotique, peuvent augmenter son absorption, permettant de ne pas surdoser en fer.
Est-ce que cette formule a la même efficacité sur le fer héminique et non héminique alimentaire ?
Non. Notre formule sera efficace sur le fer non-héminique car c’est l'absorption de cette forme de fer qui a besoin d’être optimisée. En effet, le fer héminique, en étant intégré dans l'hème (noyau des globules rouges), est naturellement bien absorbé par un transporteur qui lui est spécifique. Le fer non héminique ne bénéficie pas de ce transporteur et est beaucoup moins bien assimilé.
Puisqu’il est difficile d’identifier un déficit en fer par des symptômes, est-ce que je dois me supplémenter préventivement ?
Il faut noter que si les symptômes de manque de fer sont difficiles à identifier, on peut néanmoins facilement repérer un déficit ou une carence via analyses sanguines (contrairement au magnésium par exemple). Il est ainsi déconseillé de se supplémenter préventivement en fer, surtout si on ne fait pas partie des populations à risque (notamment les hommes).
Dans tous les cas, si vous pensez manquer de fer, nous vous recommandons de vous rapprocher de votre médecin et de doser votre ferritine.
Votre complément est-il compatible avec un médicament pour un traitement lié à une carence en fer ?
Si vous prenez déjà un traitement contre l’anémie, la prise d’un complément supplémentaire sera redondant. Parlez-en avec votre médecin.
Une carence en fer se ressent-elle physiquement ?
Pas forcément. Les symptômes de la carence en fer sont mal définis et ceux de l’anémie sont bien plus marqués, comme une fatigue importante. Avant de risquer l’anémie, il est donc possible de faire préalablement analyser l’état de ses réserves en fer (via un dosage sanguin de ferritine) pour évaluer si une carence en fer est présente.
On dit qu'il ne faut pas boire de thé après un repas pour optimiser l’absorption du fer, est-ce vrai ?
Oui, absolument. Les polyphénols (tanins) du thé (qu’il soit vert ou noir) complexent une partie du fer de notre alimentation qui n’est alors plus libre pour être absorbé et stocké dans l’organisme. Si vous êtes dans une démarche d’optimisation de vos apports en fer, il est préférable de consommer le thé en dehors des repas et de ne pas prendre votre supplémentation avec vos tasses de thé.
La souche permet-elle d'absorber le fer végétal ou animal ?
Notre formule sera efficace sur le fer végétal, non héminique. Le fer animal, sous forme héminique, est une forme de fer directement absorbée par l’intestin via un transporteur spécifique de l’hème. C’est pourquoi il est intéressant d’optimiser l'absorption du fer végétal, dont l'absorption est moins importante.
Constipation, diarrhées… Quels sont les effets secondaires d’un supplément en fer ?
Certaines formes de fer peuvent provoquer des troubles digestifs. Évitez les sulfates, fumarates, ascorbate ou encore gluconate et privilégiez le bisglycinate.
Pourquoi n’avoir pas utilisé des gélules gastro résistantes dans votre formule alors qu’il y a un probiotique ?
L’absorption du fer se fait essentiellement dans la partie haute de l'intestin grêle (juste après l’estomac). C’est pourquoi, la libération du fer et de la souche lactique Lactobacillus plantarum 299vⓇ doit être faite suffisamment tôt. Or les gélules gastro-résistantes favorisent une libération tardive, au niveau du côlon, ce qui est incompatible avec l’objectif de notre formule d’améliorer l’absorption du fer. C’est pour cette raison que nous utilisons des gélules HPMC simples et à libération rapide. D’ailleurs, les études cliniques sur la formule ont été réalisées précisément avec ce type de gélules !
Pharmacie, site.. où trouver ou acheter notre complément alimentaire Fer Bisglycinate ?
Vous pouvez naturellement acheter notre Fer Bisglycinate au meilleur prix directement depuis notre site Internet. Vous pouvez également acheter notre complément alimentaire de fer en pharmacie au prix identique (sans ordonnance) et dans certaines enseignes spécialisées.
Retrouvez nos dossiers et articles relatifs au Fer

Comment faire une cure de fer et pourquoi ?
Dans quels cas faire une cure de fer, comment la réussir et surtout, quels sont ses effets sur la santé ?

Les aliments riches en fer
Animale, végétale… en fonction de la source, la forme de fer n’est pas la même et surtout, son absorption sera différente.

Alimentation en cas d’anémie
Si vous avez tendance à faire de l’anémie, quels aliments peuvent contribuer à optimiser vos apports en fer ?
Paiement
sécuriséLivraison offerte
dès 69€ d'achatLivraison
en 48hParrainer
un procheRécompenses
fidélité

Inscrivez-vous à nos communications et bénéficiez de contenus exclusifs, du programme fidélité et d’offres personnalisées.