Ce qu'il faut retenir :
- 9 causes principales ont été identifiées comme étant à la base du vieillissement cellulaire, qui finit par induire des signes visibles ou des maladies.
- Certaines Biotechs sont déjà sur le coup, et s’essayent aux thérapies géniques pour ralentir ce processus inéluctable.
Vous pensez qu’un article sur le vieillissement ne vous concerne pas. Vraiment ?
Évacuons d’emblée la question qui fâche : non, un article sur le vieillissement ne s’adresse pas uniquement à celles et ceux qui se regardent tous les matins dans le miroir en pensant la même chose : « elle n’y était pas hier elle, si ? ». Qu’il y ait des signes visibles ou non, le vieillissement nous concerne tous. Au-delà des aspects visibles, métaphysiques et psychologiques, se cache une réalité microscopique commune à l’ensemble du vivant : le vieillissement cellulaire. Ce processus froid et implacable se matérialise par des mécanismes complexes liés à notre patrimoine génétique, soit à la source même de tout ce qui nous caractérise (1).
Derrière les marques visibles du vieillissement se trouve un processus dont on commence à peine à entrevoir les mécanismes, et qui démarre à l’échelle de notre ADN…
Comment est-ce que nos cellules vieillissent ?
La question du vieillissement fascine l’être humain depuis toujours, et la raison paraît évidente : identifier les causes « originelles » du vieillissement ouvrirait la voie à une intervention directe qui pourrait mener au Graal absolu : la vie éternelle. Mais rassurez-vous, on n’y est pas encore, même si certains y ont cru très fort dans les années 90 (vous vous souvenez de la DHEA ?). Comme souvent, faisant fi de l’agitation, la recherche avance. Récemment, une étude parue dans la revue CELL a mis en lumière les 9 empreintes du vieillissement cellulaire (2). Ces 9 phénomènes qui ont lieu au fin fond de vos cellules conduisent in fine au rituel matinal évoqué ci-dessus, voire à certaines maladies. Accrochez vos ceintures, ça va devenir technique, mais c’est pour la bonne cause.
9 causes cellulaires ont récemment été identifiées comme à l’origine du processus de vieillissement.
Les marques primaires : le vieillissement à l’échelle de notre ADN
1. L’instabilité génomique. Les lésions sur notre ADN s’accumulent avec l’âge et altèrent le code qui permet aux cellules de se reproduire, causant donc des dysfonctionnements cellulaires majeurs.
2. La réduction des télomères. Vous avez entendu parler d’Elisabeth Parrish ? Pardon « Liz’ » Parrish ? Elle dirige une start-up dont la technologie génomique permettrait d’allonger nos télomères et de freiner le vieillissement. Les télomères protègent l’extrémité de nos chromosomes. Avec l’âge ils se détériorent, le chromosome est exposé et peut s’altérer. Un chromosome altéré transmet mal l’information génétique causant des erreurs fatales. Pour la petite histoire, Liz’ (ça va on est copains) s’est fait appliquer son traitement dans une clinique secrète aux US. On vous laisse juger du résultat. La découverte des télomères et leur impact sur le vieillissement a tout de même abouti à un prix Nobel en 2009 pour E. Blackburn (3,4). Comme quoi Liz’ sait très bien ce qu’elle fait.
3. Les altérations épigénétiques. Une altération épigénétique c’est comme un bout de scotch posé sur un vinyle, qui ferait sauter la musique. Elle empêche votre chromosome d’exprimer la production de certaines protéines essentielles.
4. La perturbation de la protéostasie. C’est les protéines qui déraillent. Leurs fonctions et caractéristiques sont perturbées, entrainant agrégation, accumulation voire toxicité (5).
La dirigeante de la start-up américaine BioViva s’est injecté un traitement génomique qui a allongé ses télomères. Elle affirme ainsi avoir biologiquement rajeuni de 20 ans.
Les marques secondaires : conséquences directes des marques primaires
5. La dérégulation de la détection des nutriments. Le corps ne sait plus bien utiliser les nutriments, ce qui peut mener à certaines maladies (par exemple : diabète).
6. Dysfonctionnement des mitochondries. Ces petites centrales énergétiques sont cruciales dans le fonctionnement de l’organisme. Perturbation des mitochondries = dérèglement cellulaire assuré.
7. La sénescence cellulaire. L’accumulation d’erreurs dans leur reproduction aboutit à des cellules endommagées voire non-fonctionnelles.
Les causes finales : les plus « visibles »
8. L’épuisement des cellules souches. Une diminution des cellules souches, c’est une accélération assurée de la dégradation des tissus (musculaires, osseux, nerveux, de la peau…).
9. L’altération de la communication cellulaire. Avec l’âge, les cellules communiquent moins bien entre elles (hormones, molécules du système immunitaire…), et ne réagissent plus efficacement en cas de besoin (inflammation, détection de toxiques…).
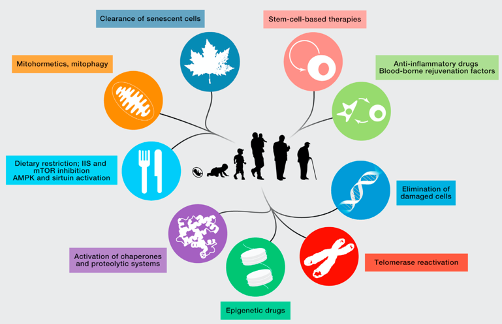
tirée de (2)
Pour tous ceux qui ne croient pas (encore) en la thérapie génique pour rajeunir, une alimentation saine, riche en antioxydants, et la nutraceutique sont un bon début.
« Vieillir trop vite » non merci !
Vous l’aurez compris, le vieillissement est un processus complexe et multifactoriel. Bien qu’au cours du vieillissement, les capacités de défenses de l’organisme diminuent de manière naturelle (6), nous ne sommes pas tous égaux face à cette mécanique cruelle : stress, pollution, facteurs alimentaires, niveau d’activité physique... impactent le vieillissement. Et si nos modes de vie sont une clé indéniable, il existe des solutions qui permettent d’aider le corps à ralentir ce processus. Une alimentation équilibrée est une option (bien difficile à mettre en œuvre parfaitement), la nutraceutique peut venir en soutien (7,8). Pas besoin d’appeler Liz’ pour se faire injecter un traitement génomique dans une clinique ultra-secrète aux États-Unis !
Publications
1. de Jaeger, C. Physiologie du vieillissement. EMC 2017, 26-007-D-10, 11.
2. López-Otín, C.; Blasco, M.A.; Partridge, L.; Serrano, M.; Kroemer, G. The Hallmarks of Aging. Cell 2013, 153, 1194–1217, doi:10.1016/j.cell.2013.05.039.
3. Kahn, A. Télomères, maladies et vieillissement. médecine/sciences 2005, 21, 451–452, doi:10.1051/medsci/2005215451.
4. Blackburn, E.H.; Epel, E.S.; Lin, J. Human telomere biology: A contributory and interactive factor in aging, disease risks, and protection. Science 2015, 350, 1193–1198, doi:10.1126/science.aab3389.
5. Korovila, I.; Hugo, M.; Castro, J.P.; Weber, D.; Höhn, A.; Grune, T.; Jung, T. Proteostasis, oxidative stress and aging. Redox Biol. 2017, 13, 550–567, doi:10.1016/j.redox.2017.07.008.
6. Tan, B.L.; Norhaizan, M.E.; Liew, W.-P.-P.; Sulaiman Rahman, H. Antioxidant and Oxidative Stress: A Mutual Interplay in Age-Related Diseases. Front. Pharmacol. 2018, 9, 1162, doi:10.3389/fphar.2018.01162.
7. Conti, V.; Izzo, V.; Corbi, G.; Russomanno, G.; Manzo, V.; De Lise, F.; Di Donato, A.; Filippelli, A. Antioxidant Supplementation in the Treatment of Aging-Associated Diseases. Front. Pharmacol. 2016, 7, doi:10.3389/fphar.2016.00024.
8. Mc Auley, M.T.; Guimera, A.M.; Hodgson, D.; Mcdonald, N.; Mooney, K.M.; Morgan, A.E.; Proctor, C.J. Modelling the molecular mechanisms of aging. Biosci. Rep. 2017, 37, BSR20160177, doi:10.1042/BSR20160177.










